개요
- 2013년 설립한 CTC(Circulating Tumor Cell)기반 Liquid Biopsy 장비, 솔루션 기업이다.
- 13년간 적자를 냈으나 계속해서 투자를 받음. 결국은 자금문제로 켄디엑스홀딩스가
최대주주 등극. 13년간 적자를 낸 기업을 인수한 이유는 회사의 기술력에 주목한 것.

- 켄디엑스 홀딩스는 2023년 말 싸이토젠의 최대주주가된 SPC로, 엑셀시아캐피탈 코리아가 설립한 펀드로 엑세스바이오,메리츠증권이 주축으로 참여. 구주와 신주 CB 인수에 총 1155억원을 투입한 딜이다.
- 24년 말부터 하여 25년까지 매출의 퀀텀점프가 일어나며 적자폭이 줄어들고 있다.
- 거기다가 26년은 미국 쪽 규제 철폐로 CLIA LAB 매출의 성장을 기대하게 되어, 싸이토젠이 드디어 영업레버리지 구간에 들어가는 초입인 것으로 보인다.

- 2021.1Q ~ 2025.3Q까지 분기별 싸이토젠 별도 매출, 연결매출, 연결 영업이익 추이이다.

- 2022.2Q 부터 종속기업 편입.
- 2022.4Q에 ExperTox, 지놈케어를 인수, 종속기업으로 편입되면서 연결 매출 상승폭 커짐.
- 특히 산전 유전자 진단을 하는 지놈케어의 매출 비중이 더 큼
- CLIA lab(실험실 표준 인증)인 미국의 ExperTox의 인수는 미국 진출의 교두보
- 2024.3Q에 다시 Top line 래벨 업
- 2025년 3분기 누적매출은 창사이래 최대치를 기록하며 영업적자 폭을 대폭 줄여가는 중. 26년 하반기에는 분기 BEP를 달성할 것으로 예상되며 27년은 영업레버리지 효과가 터지는 구간 진입
< 종속기업 현황 (2025.3Q) >


CTC진단이란?
- Liquid Biopsy(액체생검)의 한종류
- 액체생검이란 일반적으로 혈액속에서 ctDNA(순환 종양 DNA)나 CTC(순환 종양 세포), 엑소즘을 분리하여 ctDNA는 DNA Seq, CTC, 엑소즘은 DNA Seq, RNA Seq, protein 검사등을 하여 암조직으로 CT에 보이기 8개월 전에 디텍팅이 가능
- 암이라는 것은 십억개의 세포가 뭉칠때 CT나 현미경으로 확인 가능함.
- 근데 혈액속에서 돌아다니는 암세포나, 암세포의 DNA 조각을 찾아만 내면 조기치료 가능
-액체생검은 조기진단, 동반진단, MRD의 장점이 있다.
- 액체생검은 비침습성, 반복 용이성, 다양한 세포나 DNA를 본다는 면에서 높은 정확성, 조기진단이나 전이전에 본다는 면에서 암치료의 성공률을 비약적으로 높임
- 실제 암환자의 90%는 원발암 보다 전이암으로 사망
- CTC는 혈액 1ml에 10억개의 혈구세포 중에 10개 미만이 있는데 그것을 산채로 분리한다는 것은 엄청난 허들임
- 너무나도 많은 장점에도 불구하고, 민감성과 특이성이 떨어지는 것과 분리기술의 허들로 비용문제 때문에 그동안 상용화가 느려졌음
-그러나 기술발전으로 민감성, 특이성 ,분리기술 문제가 해결되고 있고, 싸이토젠은 이제 상용화의 노크를 두드릴때가 생각해서 미국에 CLIA lab을 인수하고 미국 시장에 진입함.
-ctDNA와는 아래와 같이 비교할 수 있다.
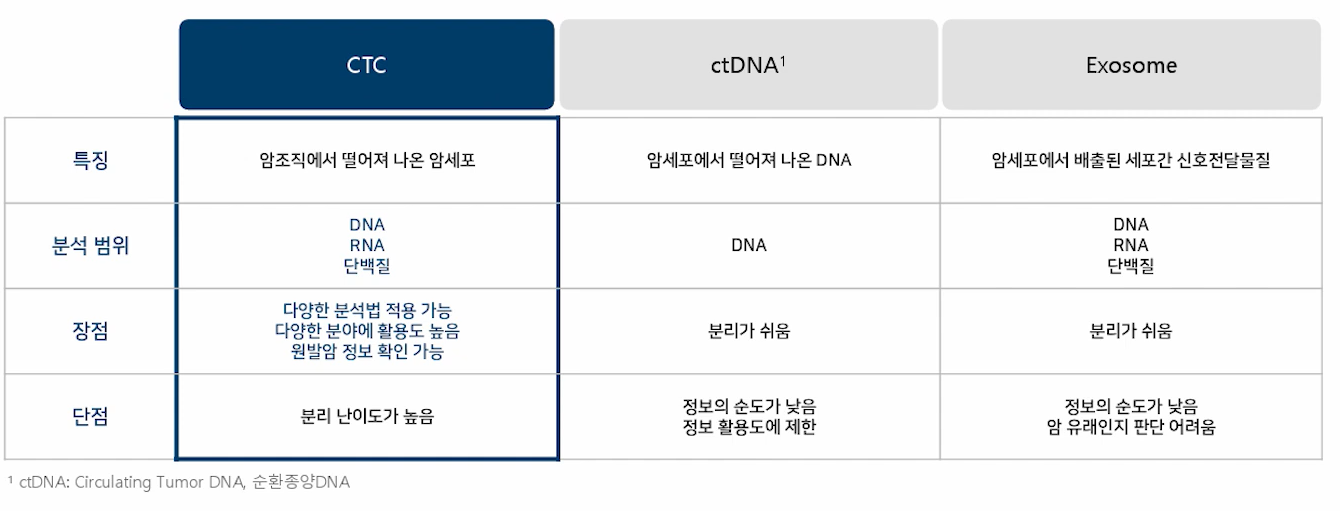

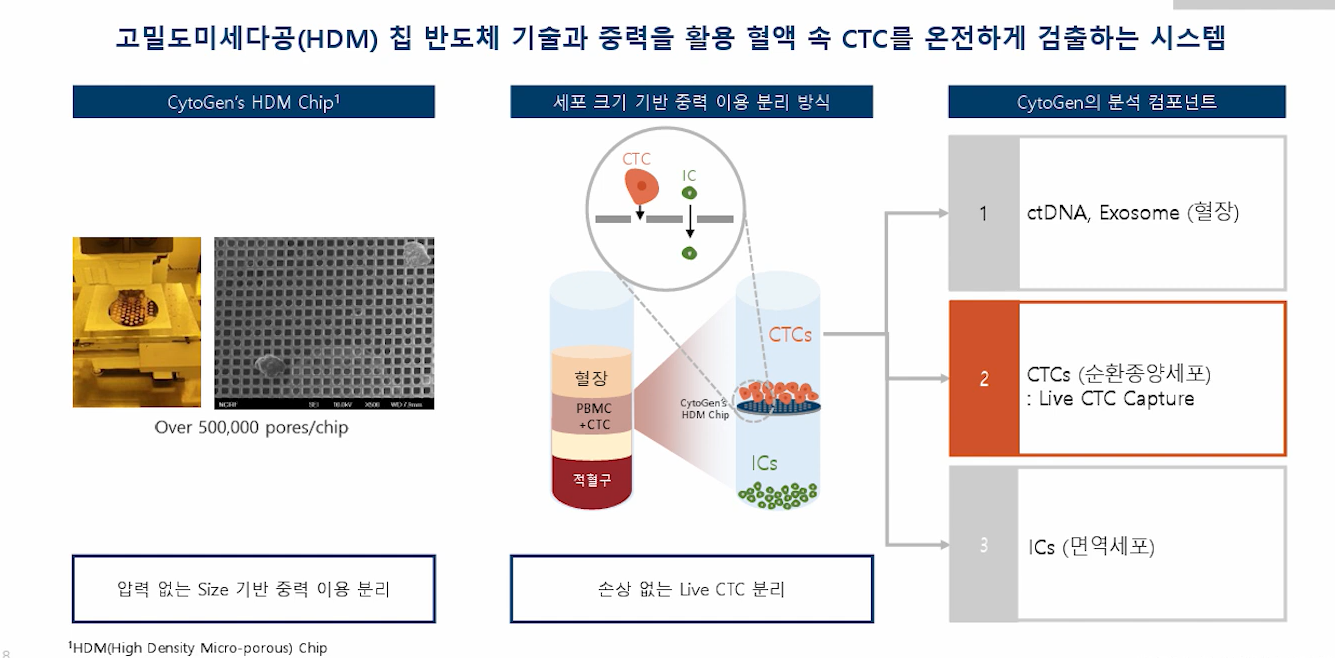
- 싸이토젠의 분리기술은 HDM에 있다.
투자 포인트
- ExperTox (미국 CLIA lab)

Exper Tox의 BM은 크게 두가지다.
1) 미국내에서 직접(Direct) 진단 서비스
- 22년 인수한 CLIA lab으로 미국 대형병원 대상으로 CTC 진단 서비스 제공
- Exper Tox는 미국 병리학회(CAP)인증을 보유하고 있어 미국 대형병원 수준의 진단 검사 신뢰성을 확보.
- FDA 인증을 안받고 우회해서 CLIA LAB으로 들어가는 것은 임시 대응? 반은 맞고 반은 틀리다.
- CLIA lab이란 임상실험실 표준인증제도 인증을 받은 실험실로 미국 연방 규정을 준수하는 시설을 의미하며, FDA에 의료기기 허가없이도 대형병원을 상대로 의사진단을 받은 환자에게 직접적으로로 진단서비스 가능.
- CLIA lab에서 하는 IVD(체외진단 서비스)를 LDT(Laboratory Developed Test)라고 말한다.
- LDT는 단일 실험실 내에서만 FDA의 허가없이 설계, 제조 및 사용되는 체외진단 서비스를 의미한다.
- LDT의 장점은 비용 효율적이며, FDA 인증 같은 규제를 피해서 시간을 절약하며, 빠르게 변하는 최신기술을 UPDATE하여 바로 적용할 수 있다.
- 요즘 대형병원들은 FDA 인증을 받아서 단가도 비싸고 시간도 오래 걸리고, 현 기준으로 시간이 지난 기술이 적용된 기기를 쓰기보다, 자체 CLIA LAB을 만들거나 외부 CLIA LAB에 아웃소싱을 주는 방식으로 체외진단 서비스를 하는 경우가 많다.
- 이로써, CLIA LAB에서 FDA 510K 승인없이도 의사의 처방이 있으며 CTT 진단서비스가 가능. FDA 규제 장벽을 우회해서 들어감.
- 의사의 처방을 받고 환자나 보험사에 직접 청구하는 B2C 사업 모델이 가능
- 사업 확장의 포인트는 결국 의사의 처방전을 받아 환자에게 직접 청구하기 위해서는 CPT 코드를 부여받고 사보험에서 수가를 책정받아아 보험승인 사례를 만들어 줘야함.
- 현재 미국의 시더스사이나이 병원에 CTC 분석 서비스를 제공중이며, MD 앤더슨 암센터, UCLA등 미국 주요 의료기관과 스마트 바이옵시 플랫폼 공급을 협의 중이다.
- 최근 리스크는 FDA에서 LDT(실험실 개발 테스트) 규제를 하였으나, 2025년 3월 텍사스 지방법원에서 FDA의 최종 규정을 무효화. FDA는 25년 9월, 1년 반만에 규제를 철회.
- FDA의 규제 리스크 때문에 24년 부터 CTC 진단 서비스 계약은 연기되었고, 기존에 하던 독성진단 서비스만 유지하며 버팀.
- 하지만, 26년 부터는 CTC 체외진단 서비스뿐만 아니라, 대형병원, 연구소와 이어지던 협의가 실질 계약으로 이어질 것으로 기대
- 2013년 부터 CTC 테스트에 대한 CPT 코드가 존재하기 때문에, Exper Tox를 통한 보험청구 전략을 구체화 하는 중.
- 일본 NCC하는 암연구와 다이치산쿄등 글로벌 제약사와의 협력이 결실을 보일때가 됏다.
2) CLIA LAB , 대학 암센터, 연구소, 병원에 판매 공급
- 장비를 거의 마진없이 판매 후, 소모품이나 진단서비스로 반복매출을 올리며 고객 확대할려는 전략이 기본
- 물론, FDA 의료기기 인증을 아직 안받은 상황이라 시장에서 판매는 불가. 대형병원의 LDT(Laboratory Developmentet Test)를 하는 자체 CLIA LAB이나, NIH와 같은 연구소에 환자 진단용이 아닌 연구용으로 판매
- 현재 추세가 in vitro test의 경우 신속하고 최신 updated tech 장비를 사용하기 위해 CLIA LAB 이용이 주류임. 따라서 CLIA LAB 대상 마켓팅이 임시적인 대응이 아님.
- 추후 FDA 의료기기 510K 승인도 받을 것.
- 앞에서 보험확대가 중요하다고 언급했는데, 그러기 위해서는 임상시험에 많이 쓰이면서 논문이 쏟아져 나오고 -> 이 근거를 바탕으로 의사 처방이 나오고 -> 질병코드 CPT가 나오고 private payer가 급여를 적용해주는 선순환 구조가 나와야 한다.
- 그런면에서 대형병원, NIH, 대형 암센터에 싸이토젠의 장비가 다른 회사 장비 대비 비교우위를 가지고 채택되는 것은 선순환 구조의 출발점이다.
- 미국 서부 대학 암센터인 UCLA와 USC에 공급. 이들 기관은 Single cell RNA Sequencing 기반 연구에 싸이토젠의 CTC 분리 기술 사용. NIH(미국 국립 보건원)에 2022년 공급
- 어쨌던 제일 중요한 포인트는 Top line이 올라가야함.
2. NIH ,NCC 및 글로벌 제약사와의 파트너쉽
- NIH, 그 중 암 면역요법의 아버지라 불리는 스티븐 로젠버그 박사의 연구소에 액체생검 플랫폼을 공급함
- 로젠버그 박사는 세포 치료제(CAR-T, TIL등)연구를 주도하고 있는데 여기에 싸이토젠의 CTC 분리, 분석 기술이 녹아들어간 장비가 쓰여짐. 추후 빅파마에게 강력한 레퍼런스임
- 27년 200조원 규모로 성장할 것으로 예상되는 면역함암제 시장의 핵심 모니터링 툴로 사용된다는 뜻
- 면역항암제는 환자마다 반응이 다르기 때문에, 치료 효과를 실시간으로 모니터링하는 바이오마커의 중요성이 높음.
https://www.mk.co.kr/news/stock/11022056
- Single Cell RNA Sequencing을 기반으로 하는 미국에서 가장 큰 액체생검 센터인 USC에 싸이토젠의 Smart Biopsy ™ Platform을 공급한다. 이를 활용해 CTC를 회수해서 오가노이드 배양 기술과 접목하여 전립선암 최적의 항암제를 선택하는 동반진단 툴로 사용할려고 한다.
- CEPM(뉴욕정밀의료센터) , NCC(일본 국립암센터)등이 싸이토젠의 플랫폼으로 임상을 진행중이다.
- 이 밖에 미국 상위 암병원인 Cedars-Sinai와 공급계약을 체결하는 등 대형병원과의 계약이 이어지고 있다.
3. AACR(미국암연구학회)에서 발표된 임상데이터 유효성
- 2025년 4월 시카고에서 열린 AACR에서 싸이토젠의 기술의 상용화 가능성을 높여줌
- 전립선암 환자의 혈액 속 CTC에서 ‘AR-V7’이라는 바이오마커를 검출하는 기술을 발표
- AR-V7이 발현된 환자는 일반적인 호르몬 치료제에 내성을 가지므로, 이를 선별하여 치료제를 변경하는 등 대응을 하여 비용과 시간을 아끼고 치료 효과를 높여줌
- 이는 기존의 조직 생검으로는 확인이 불가한 바이오마커를 액체생검으로 해결하여 미충족 수요를 공략
- 그리고, 뼈 속에 암세포가 증식하는 다발성 골수종은 진단을 위해 극심한 고통을 수반하는 골수 천자를 반복해야함. 싸이토젠은 이를 혈액검사로 대체하여 환자의 고통을 줄여주고 반복적인 검사가 가능하여 MRD(미세잔존질환) 모니터링이 가능
4. 나테라, 가던트헬스에서 보는 투자아이디어
- 미국의 대표적인 액체생검 기업인 나테라와 가던트헬스 주가 행보가 다르다.
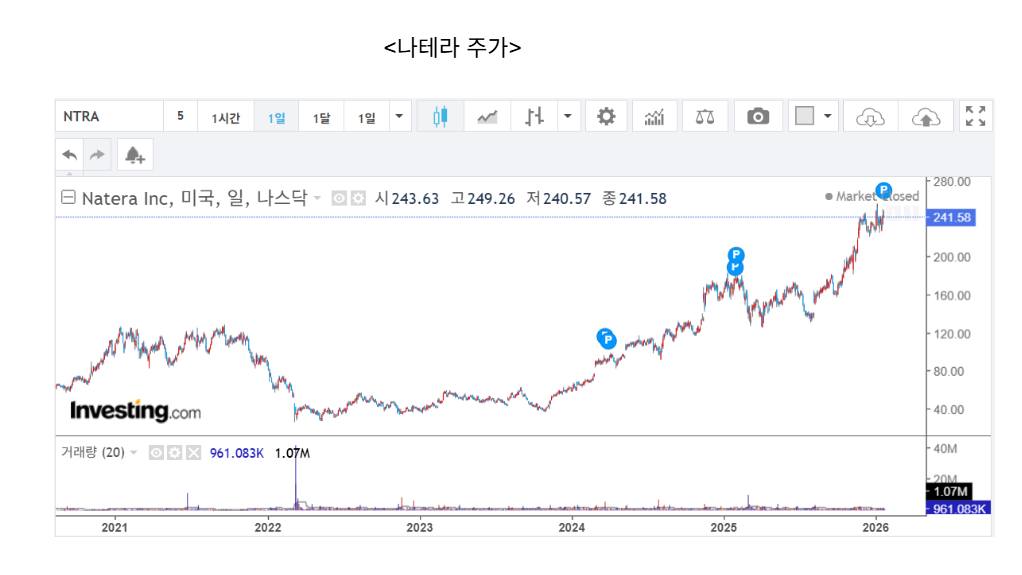

- 나테라는 승승장구 하고 있고, 가던트헬스는 최근 턴어라운드로 살아나고 있지만 한발 뒤쳐져 있다.

. 나테라
- 나테라는 MRD 시장을 장악. 조직생검 + 액체생검(ctDNA)으로 개인 맞춤형 정밀진단을 제공
- Signatera는 조기진단 스크리닝 검사가 아니라 진행성 암 환자 대샹으로 우선 조직검사를 하여 유전자 분석하여 돌연변이 16개를 찾아낸다.
- 16개의 돌연변이를 찾을 수 있는 환자 맞춤형 시약을 만든다.
- 그 다음 부터는 병원갈때 혈액을 채취하여 맞춤형 시약으로 액체생검을 하여 16개 돌연변이가 있는지 확인하여 MRD 위험성을 판단
- 전이되기전에 액체생검으로 진단하기 때문에 CT보다 8.7개월 먼저 재발여부 진단 가능함
- 대다수의 항암 임상시험이 Signatera를 gold standard로 채택
. 가던트헬스
- ctDNA로 정밀진단을 제공하려고 하나 민감도와 특이도에서 나테라의 조직생검+액체생검에 크게 밀림
- ctDNA 기반으로 조기검진(screening) 시장에 사활을 걸었음
- ctDNA의 장점은 혈액을 채취하여 NGS로 자동화가 가능하지만 혈액내 모든 DNA를 하나씩 ,한개당 예를들어 10번씩 ultra deep seq을 해야해서 비용이 많이듬. 근데 ctDNA가 DNA의 분리조각이어서 민감도도 떨어지는편이나 기술발달이 되면서 극복해 나가는 중
- 최근 대장암 조기진단 서비스 개화 가능성이 보임
. 나테라의 Signatera의 한계점은?
- 암은 heterogeneity하고 돌연변이는 계속 발생한다. 맨처음 조직검사한 돌연변이가 계속 유지된다고 확신못한다. 새로운 돌연변이 발생한 것에 대해서는 대응 못함
- 조직검사를 또 하면 된다고? 그럴거면 병원올때마다 조직검사를 햐면 되는데 뭐하러 ctDNA로 액체생검을 하나? 왜냐면 조직검사는 구조적으로나 위험한 면 때문에 30%는 조직을 못뗴어냄. 그리고 조직 생검은 환자에게 고통을 주고 부작용이 발생. 또한 비용 시간에서도 약점. 현실적으로 주기적인 조직생검이라는 것은 불가능함
- 액체생검은 혈액검사이므로 조직검사의 단점을 커버함. 다만, 민감도와 특이도 비용에서 극복해야할 허들이 존재함. 나테라는 ctDNA에서 그런점을 해결해 나가는 중.
- 그런데 ctDNA는 돌연변이 체크 시약에는 반응을 잘하지만, 죽은 암세포의 DNA 분리조각이라서 DNA 시퀀싱의 민감도가 떨어지고 하더라도 유전자 돌연변이 중에 현재 발현된 것은 알 수 없다.
- 하지만 CTC ( Circulating Tumor Cell)은 온전한 암세포가 혈액속에 흐르는 것으로, 이를 혈액속에서 분리만 한다면, DNA, RNA, Protein level test가 모두 가능하여 현재 혈액속에 흐르는 암세포의 상태를 가장 정확하게 알 수 있다. 조직생검을 대체하여 MRD검사를 잘할수 있고, 동반진단에도 유용함
- 원발성 암보다, 전이성 암으로 사망하는 경우가 암환자의 90%이다.
- 그런데 왜 아직 CTC 진단이 rare한 것인가?
- ctDNA는 NGS로 자동화가 쉽다. 하지만 CTC는 살아있는 상태로 분리하고 배양하는 등 시간과 비용이 많이 들고 대량 처리가 어렵다.
- 혈액 1ml에 10억개의 혈구세포가 있고 그 중에 CTC는 1~10개이다. 극악의 확률이다. 이것을 또 살아서 채취해야 해야 배양하여 오가노이드 테스트도 가능하다.
- 그러나, 조기진단(SCREENING)에는 어렵지만 MRD와 같은 환자맞춤형 진단이나 연구용 시장에서는 CTC 채취만 잘된다면 나테라의 한계를 파고들 수 있는 큰 시장이 있다.
- 현재 CTC 분리에서 싸이토젠이 글로벌 1위 기업으로 평가되고 있다.
- 왜냐면, 미국 NIH와 일본 NCC의 임상연구에 채택되었기 때문
- 실제로, 싸이토젠의 스마트 바이옵시 플랫폼의 CTC 분리기술은 HDM(고집적 미세다공)칩 위에서 CTC와 IC가 중력으로 분리하는 것인데 시간 및 효율성에서 타사 대비 훨씬 좋다고 애기한다. 특히 live CTC 채취는 싸이토젠의 장점. 타사는 쉽지않음.
- 기술적 이해는 되었고, 이것이 시장에서 잘되냐 안되냐는 결국 Top line 체크로 보는 수 밖에…
5. 매출의 퀀텀점프
- 25년은 매출의 퀀텀점프가 이뤄진 해
- 24년 별도 매출 51억원에서 25.3Q 누적 195억원으로 폭발적 성장. 기업의 체급이 바뀜
- 영업손실은 107억원에서 43억원으로 절반이하로 감소.
- 이 숫자는 미국 병원에서 테스트용이나 간헐적으로 진단에 쓰이는게 아닌 본격적으로 환자진단용 매출이 발생한다는 의미.
- 26년 하반기에 분기 BEP 달성 예상
- 27년부터는 본격적인 확산이 되면서 영업레버리지가 터지는 구간으로 예상

- 현재 매출이 올라가는 사업분야는 국내 액체생검과 국내 지놈케어의 산전 cfDNA 유전진단에서 올라간다. 미국, 일본쪽 매출은 박스권

- 자회사 지놈케어 캐쉬카우 역할. cfDNA 액체생검을 통한 산전 검사 비급여 항목으로 단가 높음. 25년 하반기 부터 지놈케어는 NGS 기반 유전체 분석 서비스 신규 론칭칭
- 국내에서이긴 하지만 액체생검 본업의 매출이 개화한게 눈에 띈다.
- 국내 액체생검의 매출처는 삼성서울병원, 서울대병원,세브란스병원,서울아산병원등의 병원이며 스마트 바이옵시 플랫폼 판매. 소모품 판매가 이어지면 마진이 점점 좋아질것
- 또한 유한양행등 국내 신약 개발사에 바이오마커 발굴등 고마진 서비스
- 기대했던 Exper Tox의 매출 정체는 2024년 FDA의 LDT에 대한 규제강화 “Final Rule”발표로 LDT 불확실성이 증대에 기인한다. 당연히 규제위험은 FDA 인증을 준비해야 하는거 아닌가 하는 불안이 들면서 CTC 진단 계약은 연기되었다. 기존에 하던 독성 검사로만 매출발생.
- 하지만, 2025년3월 텍사스 법원이 FDA의 규제를 무효화하면서, 9월에 FDA는 규제를 철회하면서 26년은 새로운 도약 기대
- 26년 Exper Tox의 Top line 상승을 확인하면서 들어가도 먹을거리는 있을 것임.
- 요즘 바이오텍 분기 BEP 달성하면 시총 1조까지 가는 분위기
댓글